Trao đổi với Báo Giao thông, ông Nguyễn Ngô Quang, Phó Cục trưởng Cục Khoa học công nghệ và Đào tạo, Bộ Y tế cho biết: Về mặt khoa học, Cục đã nghiệm thu đánh giá giữa kỳ giai đoạn 3 về an toàn sinh miễn dịch và hiệu lực bảo vệ, cơ bản hội đồng đã đồng thuận để xem xét cấp phép khẩn cấp cho vaccine phòng Covid-19 "made in Việt Nam" Nanocovax. Tuy nhiên, việc quyết định cấp phép thuộc về Cục Quản lý Dược và Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc. Hiện toàn bộ hồ sơ đã chuyển sang Cục Quản lý Dược.
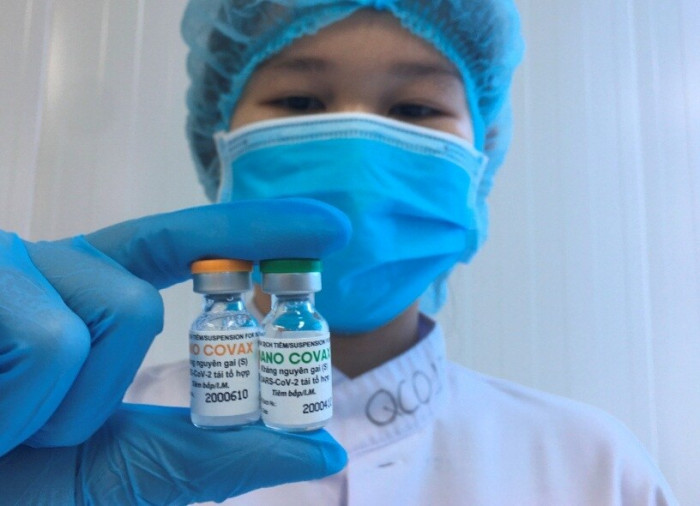
Vaccine phòng covid-19 Nanocovax đang chờ được cấp phép khẩn cấp
Vaccine phòng Covid-19 Nanocovax được các nhà khoa học của Công ty Cổ phần công nghệ sinh học dược Nanogen và Học viện Quân y nghiên cứu, phát triển, sản xuất dựa trên công nghệ tái tổ hợp, tức là sử dụng những mảnh kháng nguyên vô hại (protein) thích hợp nhất của nCoV để kích thích tạo đáp ứng miễn dịch phù hợp.
Theo thông tin trên Cổng thông tin quốc gia về doanh nghiệp, vào ngày 29/12/2021, người đại diện theo pháp luật của Nanogen đã chuyển từ ông Hồ Nhân, Chủ tịch Hội đồng quản trị sang bà Nguyễn Thị Hồng Vân, vợ ông Nhân.
Hiện bà Nguyễn Thị Hồng Vân là Tổng Giám đốc kiêm người đại diện theo pháp luật của Nanogen.
Đến tháng 3/2021, Nanogen tiếp tục tăng vốn từ 715 tỷ đồng lên 806,25 tỷ đồng.
Trong đó, ông Nhân sở hữu xấp xỉ 59,6% cổ phần với giá trị vốn góp là 480,52 tỷ đồng.
Bà Nguyễn Thị Hồng Vân đóng góp 117,8 tỷ đồng và chiếm tỷ lệ 14,61% vốn điều lệ.
Cổ đông nước ngoài có 9 tổ chức, cá nhân, trong đó, Công ty Cổ phần Chứng khoán KIS Việt Nam nắm 0,2% vốn điều lệ Nanogen (góp 1,63 tỷ đồng với lượng cổ phần nắm giữ là 162.550 cổ phiếu).
Tháng 3/2020, khi Chính phủ giao cho Bộ Khoa học và Công nghệ tìm, phân công doanh nghiệp đủ tiềm lực để nghiên cứu bào chế vaccine phòng Covid-19, công ty Nanogen chính thức khởi động.
Ngày 15/5/2020, Bộ Khoa học và Công nghệ chính thức đặt hàng Công ty Nanogen làm vaccine phòng Covid-19.
Ở thời điểm đó, ông Hồ Nhân là Chủ tịch Hội đồng quản trị, người đại diện theo pháp luật của Nanogen. Ông Hồ Nhân cũng được coi là "linh hồn", là "cha đẻ" của vaccine phòng Covid-19 "made in Việt Nam" này.
Ngày 9/12/2020, Hội đồng Đạo đức y sinh của Bộ Y tế đã họp lần cuối để xem xét, phê duyệt thử nghiệm vaccine Covid-19 trên người ở Việt Nam của Nanogen.
Vaccine này đã trải qua 3 giai đoạn thử nghiệm lâm sàng: Giai đoạn 1 bắt đầu từ ngày 18/12/2020, giai đoạn 2 từ ngày 26/2/2021 và giai đoạn 3 chính thức từ ngày 11/6/2021. Phía Bắc do Học viện Quân y, phía Nam do Viện Pasteur TP.HCM làm đầu mối triển khai.
Tháng 6/2021, Nanogen có công văn gửi Thủ tướng, xin cấp phép khẩn cấp có điều kiện vaccine Nanocovax.
Ngày 19/9/2021, Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia đã thông tin về cuộc họp xem xét kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 vaccine Nanocovax.
Theo đó, về tính an toàn, vaccine Nanocovax đạt yêu cầu về tính an toàn trong ngắn hạn dựa trên dữ liệu báo cáo kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 tính đến thời điểm hiện tại (kết quả theo dõi 7 ngày sau tiêm mũi 1 của 11.430 người tình nguyện; kết quả theo dõi 7 ngày sau tiêm mũi 2 của 5785 người tình nguyện).
Về tính sinh miễn dịch, vaccine Nanocovax có tính sinh miễn dịch dựa trên dữ liệu báo cáo kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3.
Về hiệu quả bảo vệ, theo Hội đồng vẫn chưa có dữ liệu để đánh giá trực tiếp hiệu lực bảo vệ của ứng viên vaccine Nanocovax dựa trên số trường hợp mắc Covid-19 trong nghiên cứu, cần tiếp tục thực hiện đánh giá về hiệu lực bảo vệ theo đề cương được phê duyệt.
Ước tính hiệu quả bảo vệ của ứng viên vaccine Nanocovax dựa trên dữ liệu về tính sinh miễn dịch của vaccine nghiên cứu đảm bảo tính khoa học để chuyển hồ sơ tới Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc xem xét.
Cách đây ít ngày, Văn phòng Chính phủ có văn bản truyền đạt ý kiến của Phó Thủ tướng Chính phủ Vũ Đức Đam về kết quả xem xét việc cấp giấy đăng ký lưu hành vaccine Nanocovax.
Theo đó, xét báo cáo của Bộ Y tế về kết quả xem xét hồ sơ đề nghị cấp giấy đăng ký lưu hành vaccine phòng Covid-19 Nanocovax do Công ty Nanogen đăng ký và sản xuất, Phó Thủ tướng Chính phủ Vũ Đức Đam đề nghị Bộ Y tế khẩn trương thực hiện nghiêm chỉ đạo của Thủ tướng Chính phủ theo văn bản số 1027/VPCP-KGVX ngày 17/2/2022 của Văn phòng Chính phủ và các văn bản khác có liên quan; tiếp tục hướng dẫn, hỗ trợ doanh nghiệp trong mọi trường hợp theo quy định của pháp luật.
Như vậy, sau gần 2 năm, vaccine Nanocovax vẫn đang tiếp tục chờ cơ quan chức năng xem xét cấp phép khẩn cấp...




Bình luận bài viết (0)
Gửi bình luận