Ngày 10/8, Viện Hàn Lâm Khoa học và Công nghệ Việt Nam đã tổ chức họp báo công bố kết quả nghiên cứu tiền lâm sàng thuốc VIPDERVIR điều trị Covid-19.
Tuy nhiên ngay sau đó, trên mạng xã hội chia sẻ một sản phẩm thực phẩm chức năng có thiết kế nhãn hiệu tương tự với tên gọi VIPDERVIR C. Hơn nữa đây lại là sản phẩm của Công ty Cổ phần Dược phẩm Vinh Gia là đơn vị cùng tham gia nghiên cứu loại thuốc nêu trên.
Điều này khiến nhiều người đặt dấu hỏi tại sao lại có sự trùng hợp, có thể gây nhầm lẫn giữa 2 sản phẩm này như vậy?

Viện Hàn Lâm Khoa học và Công nghệ Việt Nam đã tổ chức họp báo công bố kết quả nghiên cứu tiền lâm sàng thuốc VIPDERVIR điều trị Covid-19
Trước luồng thông tin này, trong chiều tối 11/8, Công ty cổ phần Dược phẩm Vinh Gia phản hồi bằng thông cáo báo chí. Trong đó, đơn vị này khẳng định "thực phẩm bảo vệ sức khỏe VIPDERVIR C là thực phẩm bảo vệ sức khỏe, không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh. Sản phẩm đã được công bố tại Cục An toàn thực phẩm với công dụng "hỗ trợ tăng cường sức đề kháng, hỗ trợ giảm nguy cơ mắc các bệnh do virus, do sức đề kháng kém gây ra". Sản phẩm tuân thủ mọi quy định của pháp luật về công bố và lưu hành sản phẩm, theo đại diện công ty".

Thuốc VIPDERVIR do Viện Hàn Lâm Khoa học và Công nghệ Việt Nam công bố thử nghiệm lâm sàng trên người bệnh Covid-19 nhẹ và vừa
Đơn vị này cũng cho hay "sản phẩm thực phẩm bảo vệ sức khỏe VIPDERVIR C dù đã được cấp số công bố từ ngày 29/6/2021, nhưng vì nhiều lý do chủ quan và khách quan, mà đến nay, Cty CP Dược phẩm Vinh Gia chưa tiến hành truyền thông quảng cáo cho sản phẩm này trên bất kỳ phương tiện truyền thông nào.
Sản phẩm cũng chưa được bán tại các nhà thuốc, do vậy, những tin đồn thất thiệt cho rằng Cty CP Dược phẩm Vinh Gia cố tình khiến người dân hiểu nhầm thực phẩm bảo vệ sức khỏe VIPDERVIR C là thuốc VIPDERVIR là hoàn toàn không đúng".
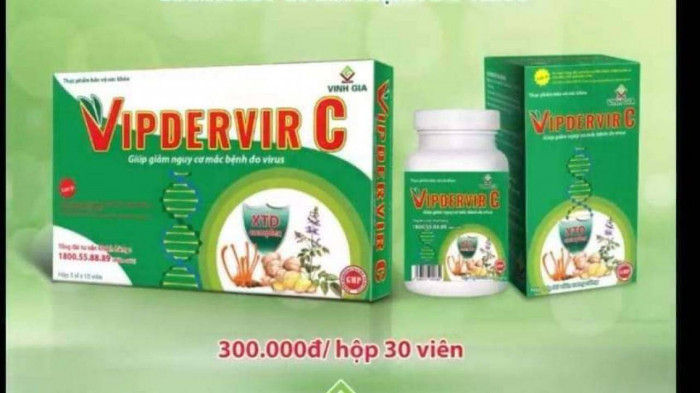
Thực phẩm chức năng VIPDERVIR-C được nhận xét có nhãn mác khá trùng với thuốc VIPDERVIR
Trước sự việc này, PV nhiều lần liên lạc với PGS.TS. Lê Quang Huấn, Viện Công nghệ sinh học, tác giả của nghiên cứu thuốc VIPDERVIR qua điện thoại nhưng chưa nhận được phản hồi.
Việc xuất hiện cùng một tên gọi (VIPDERVIR) và nhãn mác na ná nhau cho 2 sản phẩm có công dụng hoàn toàn khác nhau như vậy có bất thường? Đặc biệt khi đây lại là mặt hàng phục vụ điều trị dịch bệnh Covid-19 - đang là mối quan tâm hàng đầu của người dân hiện nay?
Trao đổi với Báo Giao thông, BS. Trần Văn Phúc (BV ĐK SaintPaul) cho rằng, điều này có thể gây hiểu nhầm cho người dân.
"Nếu cố tình gây ra sự hiểu lầm ấy, nó không đơn giản là hiểu lầm nữa mà sẽ là trục lợi, là lợi dụng các nhà khoa học để bán hàng. Việc các doanh nghiệp kết hợp với viện nghiên cứu để cho ra các sản phẩm đáp ứng yêu cầu, nhu cầu thực tiễn của đời sống là bình thường, thậm chí là được khuyến khích, để tránh tình trạng các nghiên cứu xa rời đời sống, các đề tài "đút ngăn kéo". Tuy nhiên, phải đảm bảo minh bạch, rõ ràng, nhất là với lĩnh vực liên quan đến sức khỏe con người và đặc biệt là trong bối cảnh dịch bệnh căng thẳng như hiện nay", BS Phúc nói.
Trước đó, tại họp báo, Viện Hàn lâm Khoa học và Công nghệ Việt Nam cho biết, VIPDERVIR là công trình trọng điểm của Viện Công nghệ sinh học, Viện Hàn Lâm Khoa học và công nghệ Việt Nam trong việc tạo ra chế phẩm phòng và điều trị Covid-19 từ nguồn cây thuốc Việt Nam.
Tại họp báo, PGS.TS. Lê Quang Huấn, Viện Công nghệ sinh học, đã cho biết, kết quả nghiên cứu tiền lâm sàng đã chứng minh tính an toàn và khả năng ức chế phát triển của virus cũng như tác dụng tăng cường miễn dịch.
Hội đồng Đạo đức đã đánh giá cao kết quả nghiên cứu tiền lâm sàng và chấp thuận đề cương nghiên cứu lâm sàng trên bệnh nhân Covid-19 với thuốc VIPDERVIR.
Do đó sản phẩm này được cho phép triển khai ngay giai đoạn 2, 3 trên đối tượng đích là bệnh nhân. Giai đoạn 2 sẽ triển khai thử nghiệm trên 60 đối tượng để dò liều tối ưu, chỉ định liều thuốc điều trị. Có 2 nhóm có đối chứng tham gia nghiên cứu gồm 1 nhóm điều trị phác đồ nền theo Bộ Y tế, 1 nhóm điều trị theo phác đồ nền với sản phẩm nghiên cứu. Kết thúc giai đoạn 2, sau khi đánh giá an toàn, khả năng giảm tải lượng virus của các liều và chọn liều tối ưu, Hội đồng Đạo đức Quốc gia cho phép chuyển sang giai đoạn 3 với khoảng 200 người để đánh giá so sánh giữa 2 nhóm...
Cũng tại cuộc họp báo này, ông Nguyễn Ngô Quang, Phó Cục trưởng Cục Khoa học công nghệ và đào tạo, Bộ Y tế cho biết: “Hy vọng với thời gian nghiên cứu khoảng 2-3 tháng, cùng 1-2 tháng đánh giá tổng kết, dự kiến cuối năm chúng ta sẽ cấp phép lưu hành cho sản phẩm này. Bộ Y tế sẽ phối hợp với Viện huy động mọi nguồn lực từ doanh nghiệp, nhà sản xuất, đón nhận nghiên cứu cơ bản để có đánh giá nhanh nhất, khoa học nhất, có sản phẩm phục vụ người dân”.
Báo Giao thông sẽ tiếp tục thông tin.



Bình luận bài viết (0)
Gửi bình luận